

*仅供医学专业人士阅读参考信达配资
慢病管理是一场漫长而艰辛的长跑赛,逐一把控CKD相关风险,选择心肾获益明确的药物,才能真正地延缓疾病进展。
慢性肾脏病(CKD)作为全球重大公共卫生挑战,其防治成效关乎数亿患者的生存质量与生命健康。值得欣慰的是,近年来我国在这场“对抗战”中初战告捷。最新流调数据显示,相比过去,我国成人CKD患病率下降了30%[1]。这无疑得益于医疗服务体系的完善、慢病管理的优化及新药覆盖的升级等多方面努力。
然而,庞大的患病人群基数仍不容忽视,当前我国CKD估算患病率仍达8.2%[1],且疾病负担呈持续加重趋势。权威预测表明,至2029年,每10万人中CKD患病率与死亡率将分别攀升至11.7%和17.1%[2],这极大地凸显了疾病防控的紧迫性与艰巨性。在这场关乎患者生存质量的慢病管理持久战中,选择经临床验证、具备明确心肾保护作用的治疗药物,是延缓疾病进展的关键所在。
立足预防,聚焦治疗:构建全面的CKD管理体系
第六次中国慢性病和危险因素监测(CCDRFS)显示,年龄增长、女性、少数民族、农村或中北部地区居住环境、较低的教育收入水平,以及吸烟、缺乏运动、肥胖、基础疾病(、糖尿病、血脂异常等)和有心血管疾病史等,都是CKD高危因素[1]。
将这些风险因素转化为可落地的防控行动,需多维度施策[3]:
基础疾病管理:高血压、、血脂异常是损伤肾脏的“主力军”。临床中应通过规范药物治疗,结合生活方式干预,降低血压、血糖、血脂水平,帮助肾脏减轻负担。
生活方式改善:鼓励患者戒烟,每周进行超150分钟中等强度运动;饮食遵循低盐低脂,根据肾功能合理限制蛋白摄入。
高危人群监测:针对老年人等高危群体,定期检测尿常规、血清肌酐,评估估算(eGFR),及早发现异常信号并进行干预。
社会支持构建:加强基层社区的科普宣传,优化医疗资源下沉,提供便捷服务。
除了上述预防方法之外,对于确诊后的人群,药物治疗始终是延缓疾病进程的核心防线。然而,在临床中,不少患者即便严格执药物干预,仍难以完全遏制肾功能恶化。如使用普利、沙坦类药物后,可能存在蛋白尿控制不佳或肌酐上升。因此,亟需新治疗策略应对临床难题。
药物治疗策略迎变革:延缓CKD进展为何要靶向心肾?
药物治疗策略在过去经历了明显的变革。2024年,随着改善全球肾脏病预后组织(KDIGO)CKD评估与管理临床实践指南(以下简称“指南”)的重磅发布,这场药物治疗的变革有了全新指引。时隔12年的更新信达配资,不仅凝结了CKD防治领域的前沿成果,更将治疗理念从“指标达标”提升至“改善心肾结局”[3]。为何指南会做出如此重大的调整?其原因有二。
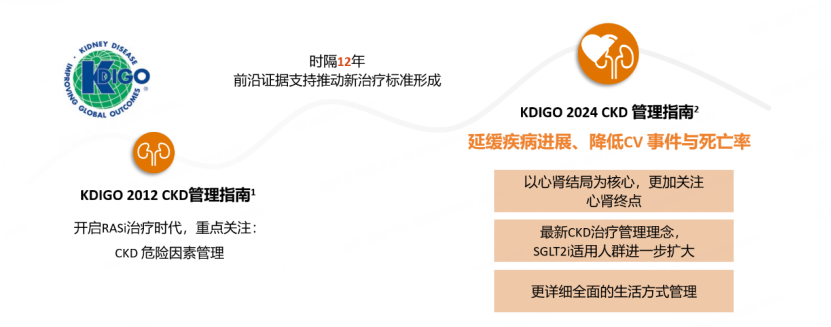
图1 KDIGO 2024更新CKD治疗理念
研究背景
一项研究数据显示,在1,200例CKD 3期患者中,约有1.8%的患者会进展至肾衰竭;而在1,276例CDK 4期的患者中,进展至肾衰竭的患者占比20.1%(如图2)[4]。也就是说,从CKD3期进展至4期,肾衰竭的风险飙升了近11倍!
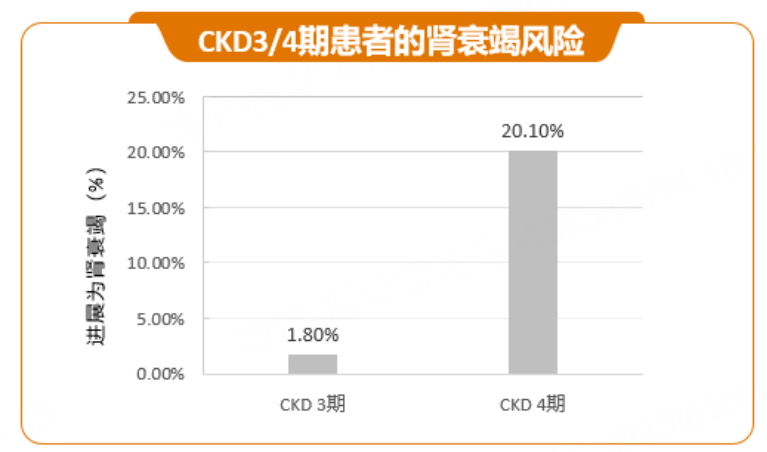
图2 CKD 3/4期患者的肾衰竭风险 [4]
2.CKD患者易合并心血管疾病,因其所致死亡率高
CKD患者具有极高的心血管风险,包括、心力衰竭、心律失常和突发性心脏死亡等,因心血管疾病而死亡的非透析依赖性CKD患者达34.7%[5]!并且在晚期CKD患者(4-5期)中,比早期CKD患者(1-3期)具有更高的心血管患病率。在CKD 5期患者中,主要致死原因不是终末期肾病(ESRD)所致肾衰竭,而是心血管疾病[6]!
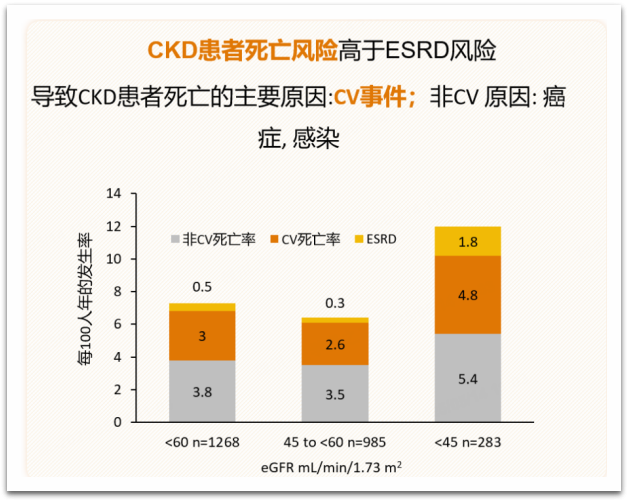
图3 CKD进展增加住院率、心血管事件发生率及全因死亡率[7]
因此,通过保护心肾从而改善心肾相关死亡,是CKD防控的目标,这是在过去十多年中的临床经验中逐步明确的。
SGLT2i引领CKD管理新目标:SGLT2i助力心肾保护,革新临床结局认知
在CKD治疗领域,钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)的出现,在很大程度上革新了CKD临床管理中对于终点目标的传统认知。CKD管理理念从“以肾病进展风险因素管理为目标”演变到“以心肾结局为中心”,追求多重获益。SGLT2i凭借独特的作用机制与显著的临床获益,为延缓CKD进展开辟了全新路径。
SGLT2i的心肾保护作用,并非依赖传统降糖机制,而是通过血流动力学与非血流动力学两大核心途径实现[8-12]。
血流动力学方面,SGLT2i能降低肾小球内压,缓解肾脏高滤过状态,减轻肾脏灌注压力,进而改善肾小球内“三高”状态(高压力、高灌注、高滤过),延缓肾小球硬化进程。此外,SGLT2i可降低间质和血浆容量,同时降低动脉僵硬度、改善内皮功能,进而减轻心脏前后负荷和心肌壁压力。
非血流动力学机制上,SGLT2i能够抑制葡萄糖、钠重吸收,减少炎症、缺氧及纤维化反应,稳定eGFR,减少白蛋白尿,从而保护肾脏。同时,SGLT2i还可改善心肌能量代谢,增加心输出量,减少心血管事件发生风险。
这些多维度的保护机制,使SGLT2i成为CKD患者延缓疾病进展、降低心肾事件风险的“有力武器”。
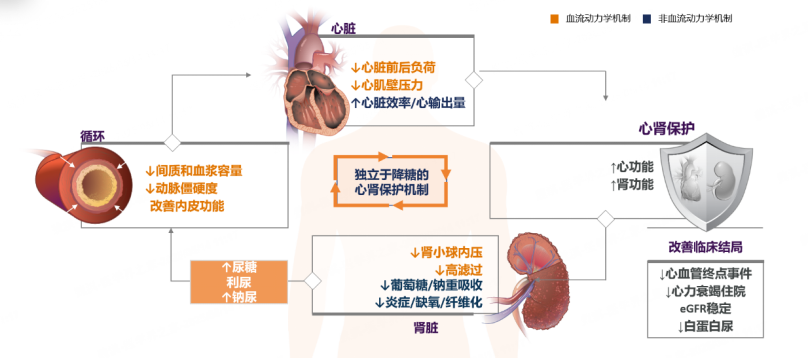
图4 SGLT2i通过血流动力学和非血流动力学机制,发挥独立于降糖机制的心肾保护 [8-12]
SGLT2i如何将上述心肾保护机制转化为患者临床获益呢?
DAPA-CKD、CREDENCE和EMPA-KIDNEY等一系列大型临床研究给出了肯定答案。这些研究不仅证实了SGLT2i在延缓CKD进展、降低心肾事件风险方面的显著疗效,更为其临床应用提供了坚实的循证医学证据。
DAPA-CKD研究数据表明,无论有无糖尿病,达格列净与安慰剂相比均可使CKD患者复合性终点事件(eGFR下降≥50%、ESRD、肾脏或心血管原因导致的死亡)发生风险降低39%(HR:0.61,95% CI:0.51-0.72;P<0.001),使肾脏特异性终点事件(持续性eGFR 下降≥50%、ESRD和肾脏相关死亡)发生风险降低44%(95% CI:0.45-0.68;P<0.001),心血管原因死亡或心力衰竭住院的复合风险降低29%(95% CI:0.55-0.92;P=0.009)[13]。
CREDENCE研究显示,与安慰剂相比,卡格列净可使主要结局[ESRD(透析、移植或持续eGFR<15ml/min/1.73m2)、血清肌酐水平倍增,或因肾脏或心血管原因死亡]风险降低30%(HR:0.70,95% CI:0.59-0.82;P=0.00001)。ESRD、肌酐水平翻倍或肾病导致死亡的肾脏特异性复合风险降低了34%(HR:0.66,95% CI:0.53-0.81; P<0.001),ESRD的相对风险降低32%(HR:0.68,95% CI:0.54-0.86;P=0.002)[14]。
EMPA-KIDNEY研究结果显示,与安慰剂相比,服用恩格列净可使CKD患者发生肾病进展或心血管原因导致的死亡降低28%(HR:0.72,95% CI:0.64-0.82;P<0.001)。格列净可使CKD患者全因住院的发生风险显著降低14%(HR:0.86,95% CI:0.78-0.95;P=0.003)[15]。
以上数据来自不同研究,人群基线不同,结果数据并非横向对比,仅供参考。
对于不同的CKD病因,SGLT2i降低肾病进展的效果如何?
SGLT2i的多靶点作用机制,使其在不同病因的CKD患者中均能发挥降低肾病进展风险的作用。
一项纳入13项大型SGLT2i试验(每组≥500例CKD患者)的Meta分析结果显示,与安慰剂相比,SGLT2i的肾脏疾病进展风险总体降低了37%(RR:0.63,95% CI:0.58–0.69)。在糖尿病患者和非糖尿病CKD患者中,SGLT2i对于肾脏疾病进展的控制无异质性(P=0.31)[16]。
对于CKD患者常见的多种病因,EMPA-KIDNEY研究分析得出,在糖尿病、肾小球疾病、高血压/肾血管疾病及其他病因的CKD患者中,SGLT2i显著降低肾脏疾病进展风险29%(HR:0.71,95% CI:0.62-0.81,P<0.001),且在不同病因的CKD患者中一致(组间P=0.62)[17]。
OPTIMISE-CKD研究和EMPA-KIDNEY研究证实,无论蛋白尿水平如何,SGLT2i均有心肾保护作用[18, 19]。
以上数据来自不同研究,人群基线不同,结果数据并非横向对比,仅供参考。
随着循证医学证据的不断积累,SGLT2i在CKD治疗中的地位也得到了国内外权威指南的高度认可(如图5)[3, 20]。从临床研究到实践指南,SGLT2i已逐步构建起从机制探索到临床应用的完整证据链,成为CKD治疗领域的重要里程碑。

图5 《中国慢性肾脏病早期评价与管理》推荐SGLT2i [3,20]
结语
CKD防控形势严峻,延缓疾病进展不仅关乎患者个体生存质量,更是减轻社会医疗负担的关键。随着临床认知的深化,治疗理念从传统的指标控制转变为以改善临床结局为核心。SGLT2i凭借独特作用机制,直接作用于肾脏靶器官,有效延缓CKD进展,显著改善患者远期预后。基于充分的循证医学证据,SGLT2i已获国内外权威指南的高度推荐,成为CKD治疗的一线药物。
参考文献:
[1] WANG L, XU X, ZHANG M, et al. Prevalence of Chronic Kidney Disease in China: Results From the Sixth China Chronic Disease and Risk Factor Surveillance [J]. JAMA Internal Medicine, 2023, 183(4): 298-310.[2] LI Y, NING Y, SHEN B, et al. Temporal trends in prevalence and mortality for chronic kidney disease in China from 1990 to 2019: an analysis of the Global Burden of Disease Study 2019 [J]. Clin Kidney J, 2023, 16(2): 312-21.[3] KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease [J]. Kidney Int, 2024, 105(4S): S117-S314.[4] DAI D, ALVAREZ P J, WOODS S D. A Predictive Model for Progression of Chronic Kidney Disease to Kidney Failure Using a Large Administrative Claims Database [J]. Clinicoecon Outcomes Res, 2021, 13: 475-86.[5] NAVANEETHAN S D, SCHOLD J D, ARRIGAIN S, et al. Cause-Specific Deaths in Non-Dialysis-Dependent CKD [J]. J Am Soc Nephrol, 2015, 26(10): 2512-20.[6] JANKOWSKI J, FLOEGE J, FLISER D, et al. Cardiovascular Disease in Chronic Kidney Disease: Pathophysiological Insights and Therapeutic Options [J]. Circulation, 2021, 143(11): 1157-72.[7] DALRYMPLE L S, KATZ R, KESTENBAUM B, et al. Chronic kidney disease and the risk of end-stage renal disease versus death [J]. J Gen Intern Med, 2011, 26(4): 379-85.[8] SATTAR N, MCLAREN J, KRISTENSEN S L, et al. SGLT2 Inhibition and cardiovascular events: why did EMPA-REG Outcomes surprise and what were the likely mechanisms? [J]. Diabetologia, 2016, 59(7): 1333-9.[9] VERMA S, MCMURRAY J J V, CHERNEY D Z I. The Metabolodiuretic Promise of Sodium-Dependent Glucose Cotransporter 2 Inhibition: The Search for the Sweet Spot in Heart Failure [J]. JAMA Cardiol, 2017, 2(9): 939-40.[10] SCHEEN A J. Cardiovascular Effects of New Oral Glucose-Lowering Agents: DPP-4 and SGLT-2 Inhibitors [J]. Circ Res, 2018, 122(10): 1439-59.[11] SHIN S J, CHUNG S, KIM S J, et al. Effect of Sodium-Glucose Co-Transporter 2 Inhibitor, Dapagliflozin, on Renal Renin-Angiotensin System in an Animal Model of Type 2 Diabetes [J]. PLoS One, 2016, 11(11): e0165703.[12] CORTINOVIS M, PERICO N, RUGGENENTI P, et al. Glomerular hyperfiltration [J]. Nat Rev Nephrol, 2022, 18(7): 435-51.[13] HEERSPINK H J L, STEFáNSSON B V, CORREA-ROTTER R, et al. Dapagliflozin in Patients with Chronic Kidney Disease [J]. N Engl J Med, 2020, 383(15): 1436-46.[14] JARDINE M J, ZHOU Z, MAHAFFEY K W, et al. Renal, Cardiovascular, and Safety Outcomes of Canagliflozin by Baseline Kidney Function: A Secondary Analysis of the CREDENCE Randomized Trial [J]. J Am Soc Nephrol, 2020, 31(5): 1128-39.[15] HERRINGTON W G, STAPLIN N, WANNER C, et al. Empagliflozin in Patients with Chronic Kidney Disease [J]. N Engl J Med, 2023, 388(2): 117-27.[16] Nuffield Department of Population Health Renal Studies Group, SGLT2 inhibitor Meta-Analysis Cardio-Renal Trialists' Consortium. Impact of diabetes on the effects of sodium glucose co-transporter-2 inhibitors on kidney outcomes: collaborative meta-analysis of large placebo-controlled trials [J]. Lancet, 2022, 400(10365): 1788-801.[17] EMPA-KIDNEY Collaborative Group. Impact of primary kidney disease on the effects of empagliflozin in patients with chronic kidney disease: secondary analyses of the EMPA-KIDNEY trial. Lancet Diabetes Endocrinol. 2024 Jan;12(1):51-60.[18] EMPA-KIDNEY Collaborative Group. Effects of empagliflozin on progression of chronic kidney disease: a prespecified secondary analysis from the empa-kidney trial [J]. Lancet Diabetes Endocrinol, 2024, 12(1): 39-50.[19] TANGRI N, RASTOGI A, NEKEMAN-NAN C, et al. Dapagliflozin Utilization in Chronic Kidney Disease and Its Real-World Effectiveness Among Patients with Lower Levels of Albuminuria in the USA and Japan [J]. Adv Ther, 2024, 41(3): 1151-67.[20] 中华预防医学会肾脏病预防与控制专业委员会. 中国慢性肾脏病早期评价与管理指南 [J]. 中华内科杂志, 2023, 62(8): 902-30.
本材料由阿斯利康提供,仅供医疗卫生专业人士进行医学科学交流,不用于推广目的。这些资料可能含有未经许可的产品/适应症的信息,阿斯利康公司不建议您将产品用于未经许可的适应症。审批编码:CN-159695 过期日期:2025-09-04
*“医学界”力求所发表内容专业、可靠,但不对内容的准确性做出承诺;请相关各方在采用或以此作为决策依据时另行核查。
兴盛网提示:文章来自网络,不代表本站观点。